在肝癌臨床試驗部分,共信已完成中國二期試驗,從病患治療結果的數據顯示,PTS藥物在中晚期肝癌治療具有顯著成效。根據衛福部統計資料,台灣肝癌為癌症死因第二名(僅次肺癌),2017年肝癌發生人數高達11,225人,為提供台灣病患更好的肝癌用藥,共信開啟台灣PTS肝癌臨床二期試驗,目前正在收案中。
[背景敘述]
本公司在中國已完成一項二期臨床試驗,對晚期肝癌病患(原發性或轉移性肝癌,病況不適合手術,或經過動脈栓塞治療後仍有腫瘤存在者),以皮膚穿刺方式進行瘤內注射PTS治療,共計收入83例患者。
[給藥過程 & 試驗結果]
病患每週進行1-3次療程,療程方式為PTS經皮膚穿刺至瘤內注射,單日注射總劑量最多為10mL。83位患者依其病況分別接受1~10次的PTS治療(病患平均治療次數為4次)。PTS瘤內注射後會造成腫瘤內部逐步消融性壞死,造成腫瘤外觀尺寸雖不變,但內部壞死比例增加的結果,最後腫瘤內壞死部位會由體內自行吸收。因此,腫瘤內部壞死部位比例可當作PTS短期瘤內注射的療效評估依據。治療完4週時,依照實體腫瘤療效(The Response Evaluation Criteria in Solid Tumors, RECIST) 標準來評估,病患的病灶(腫瘤)尺寸控制率高達72%,且腫瘤有縮小的情形。在治療成效上,腫瘤內部壞死面積大於50%的患者比例,由未接受PTS治療的16%,在接受完PTS治療後,人數上升為60% (圖一),顯見PTS在肝癌治療上具有一定的療效。
圖一、PTS中國臨床試驗二期療效分析。
[藥物安全性分析]
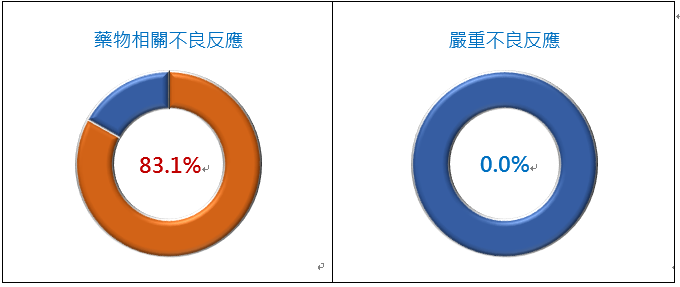
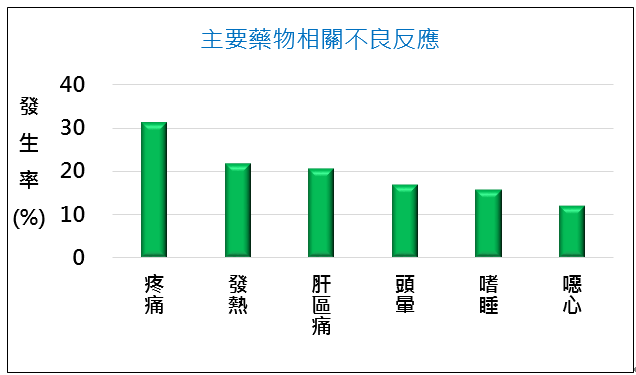
中國二期肝癌臨床試驗的受試者中,出現與藥物相關不良反應 (Adverse drug reactions) 的比例為83.1% (69/83),其中病患不適狀況需要以藥物緩解的不良反應比例為41.0% (34/83)。雖多數病患在進行PTS治療後出現不良反應,但都屬輕微副作用,並沒有嚴重不良事件(Serious adverse event, SAE) 產生 (圖二)。經PTS治療後,常見的不良反應(>10%病患會發生) 為疼痛 (31.3%)、發熱 (21.7%)、肝區痛 (20.5%)、頭暈 (16.9%)、嗜睡 (15.7%)、噁心 (12.1%),PTS藥物與傳統化療藥物相比,並沒有出現眾多副作用,如:骨髓抑制、白血球減少症及掉髮等 (圖三)。因此在用藥選擇上,PTS具有副作用較輕微的優點、能讓病患在治療後的恢復期擁有較佳的生活品質。
圖二、中國肝癌臨床二期試驗-PTS對HCC病患之安全性分析。
圖三、中國肝癌臨床二期試驗- HCC病患以PTS治療後之主要不良反應。
[個案分析-腫瘤消融情形]
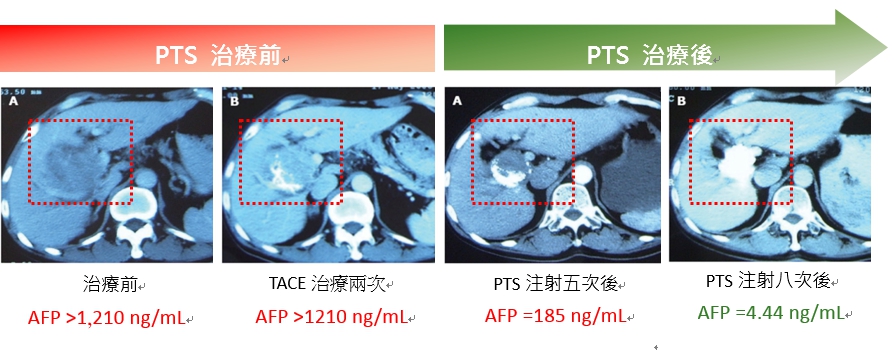
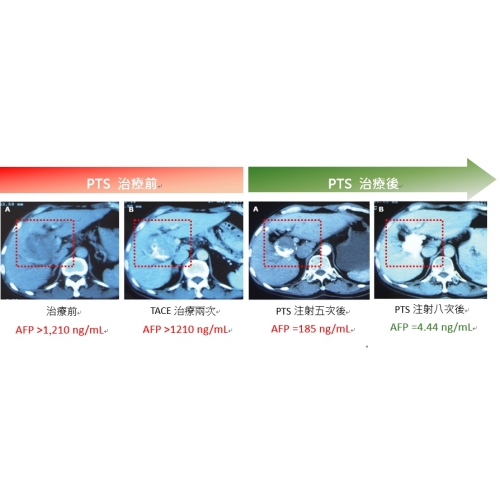
本公司在中國已完成的探索性臨床試驗[1]顯示,一位晚期有肝門靜脈侵犯的肝癌個案在接受兩次局部TACE後,影像上僅呈現有限的局部療效,個案的甲型胎兒蛋白 (Alpha-Fetoprotein, AFP, 為肝癌腫瘤標記(cancer marker)) 與TACE治療前無變化。在給予PTS治療5次後,病灶尺寸除縮小外,AFP亦大幅降低。再額外給予PTS治療3次後,病灶組織壞死且充盈著碘油顯影劑,AFP回復到正常標準。該個案接受8次PTS注射後達到病灶壞死,於其後4年沒有復發。
[註]: Alpha-Fetoprotein (AFP) 為肝癌腫瘤標記(cancer marker),是用來判別肝癌的指標。
一般正常AFP應小於20ng/ml,若數值高就有問題。
 *對於肝癌中晚期化療栓塞失效之患者,提供嶄新治療契機。(此患者經追蹤四年尚無復發情形)*
*對於肝癌中晚期化療栓塞失效之患者,提供嶄新治療契機。(此患者經追蹤四年尚無復發情形)*
本公司已於2018年取得台灣食品藥物管理署核准一項二期、劑量隨機、開放性臨床試驗,試驗目的在評估PTS用於治療不適合手術切除或現有局部區域治療的原發性肝癌患者的安全性與療效計畫,目前已在北部三家醫學中心展開此項臨床試驗。肝癌病患參加臨床試驗二期的收案標準請見臨床資訊專欄(連結在此)。
 連結點選進去後輸入關鍵字:打上PTS100
連結點選進去後輸入關鍵字:打上PTS100
【PTS100 臨床試驗發表文獻】

.PNG)