Developing an innovative “Minimally-Invasive Targeted Tumor Ablation” (MITTA) for treating focal malignancies

研究開發
核心技術 -【PTS微創靶向腫瘤消融】
PTS稱之為一種「微創靶向化學消融」(Minimally-Invasive Targeted Ablation) 的治療技術。
PTS稱之為一種「微創靶向化學消融」(Minimally-Invasive Targeted Ablation) 的治療技術。
根據一系列實體腫瘤臨床試驗(包括頭頸癌、乳癌、肺癌、肝癌等等)結果除已證實其殺惡性腫瘤的功效外,PTS的針對癌細胞殺傷性並不會引起傳統化療藥物對人體的副作用,再加上透過影像定位技術,直接將PTS注射到腫瘤的靶向性,提供相對「安全性」。
|
微創靶向腫瘤消融 |
PTS |
|
微創性 (Minimally-Invasive) |
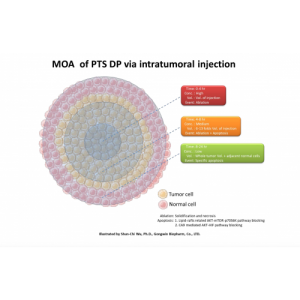
PTS結合支氣管鏡等內視鏡、影像導引 (超音波或電腦斷層) 工具定位後,以經皮穿刺等方式對腫瘤給藥。相對於傳統大傷口的開放手術 (如: 開腹手術),微創手術傷口小,術後疼痛減少、出血和感染機會也減少。術後不沾黏、不須拆線,所以復原時間短且美觀,對病人術後恢復意義重大。 |
|
靶向性 (Targeted) |
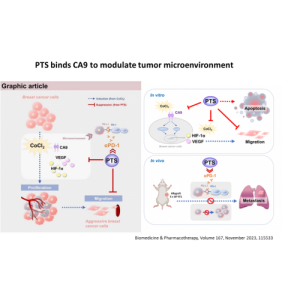
PTS為針對腫瘤部位以瘤內注射方式給藥,不擴及周圍組織;另外,依據體外研究顯示,PTS在接觸癌細胞的短時間內即可穿透癌細胞膜並大量累積在細胞質裡,其癌細胞內濃度是相對於正常細胞內的數十倍,最後造成癌細胞壞死 。直接導致作用於腫瘤組織標的,與針對癌細胞的殺傷性等兩特性,構成PTS靶向性特色。 |
|
快速消融 (Quick Ablation) |
PTS為一種化學小分子抗癌藥物,在微創介入注射24小時內即造成腫瘤細胞壞死,但對鄰近正常細胞僅有微小的傷害。 |